Математики KAIST и их сотрудники из Университета штата Флорида определили принцип того, как старение и такие заболевания, как деменция и ожирение, вызывают нарушения сна. Комбинация математического моделирования и экспериментов продемонстрировала, что скопление цитоплазмы, вызванное старением, деменцией и/или ожирением, нарушает циркадные ритмы в организме человека и приводит к нерегулярным циклам сна и бодрствования. Это открытие предлагает новые стратегии лечения нестабильных циклов сна и бодрствования.
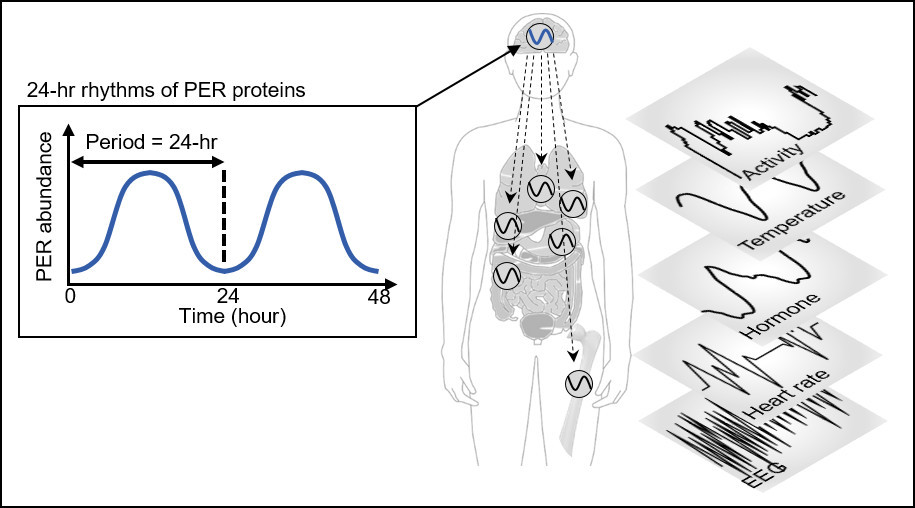
Человеческие тела регулируют режим сна в соответствии с "циркадными ритмами", которые регулируются нашей системой отсчета времени, "циркадными часами". Эти часы говорят нашему телу, когда нужно отдыхать, генерируя 24-часовые ритмы белка, называемого ПЕРИОДОМ (PER).
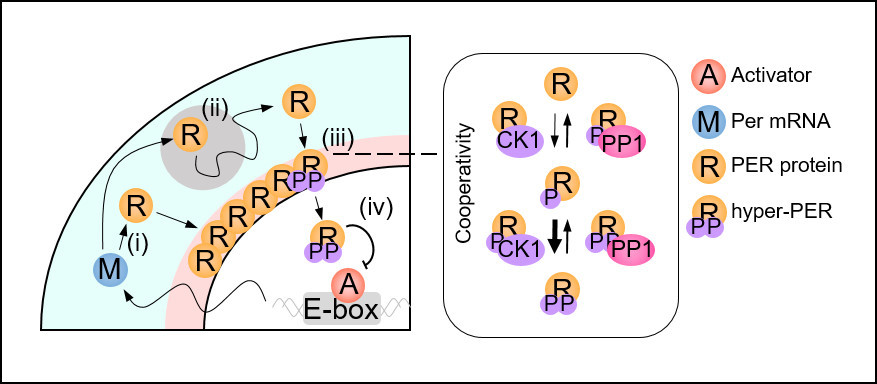
Количество белка PER увеличивается в течение половины дня, а затем уменьшается в течение оставшейся половины. Принцип состоит в том, что белок PER, накапливающийся в цитоплазме в течение нескольких часов, сразу попадает в ядро клетки, препятствуя транскрипции генов PER и тем самым уменьшая количество PER.
Однако остается загадкой, как тысячи молекул PER могут одновременно входить в ядро в сложной клеточной среде, где сосуществуют различные материалы и могут мешать движению PER. Это все равно что найти способ для тысяч сотрудников со всего Нью-Йорка заходить в офисное здание в одно и то же время каждый день.
Группа исследователей во главе с профессором Дже Кён Ким из отдела математических наук KAIST разрешила загадку, разработав пространственно-временную и вероятностную модель, которая описывает движение молекул PER в клеточной среде.
Это исследование было проведено в сотрудничестве с группой профессора Чугона Ли из Университета штата Флорида, где проводились эксперименты, и результаты были опубликованы в Proceedings of the National Academy of Sciences (PNAS) в прошлом месяце.
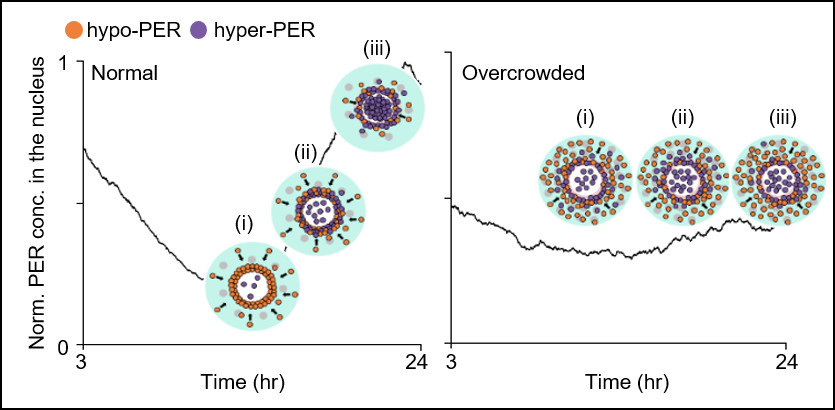
Пространственная стохастическая модель совместной исследовательской группы (изображение выше) описала движение молекул PER в клетках и продемонстрировала, что молекула PER должна быть достаточно конденсированной вокруг ядра клетки, чтобы одновременно фосфорилироваться и вместе войти в ядро . Благодаря этому переключателю синхронизации фосфорилирования тысячи молекул PER могут входить в ядро в одно и то же время каждый день и поддерживать стабильные циркадные ритмы.
Однако, когда старение и / или заболевания, включая слабоумие и ожирение, вызывают скопление цитоплазмы повышенными цитоплазматическими препятствиями, такими как агрегаты белка и жировые вакуоли, это препятствует своевременной конденсации молекул PER вокруг ядра клетки. В результате переключатель синхронизации фосфорилирования не работает, и белки PER попадают в ядро в нерегулярное время, что делает циркадные ритмы и циклы сна-бодрствования нестабильными.
Автор исследования добавляет:
Как математик, я рад помочь в разработке новых стратегий лечения, которые могут улучшить жизнь многих пациентов, страдающих от нерегулярных циклов сна и бодрствования. Воспользовавшись этими открытиями как возможностью, я надеюсь увидеть более активный обмен идеями и сотрудничество между математическими и биологическими науками.









.webp)



