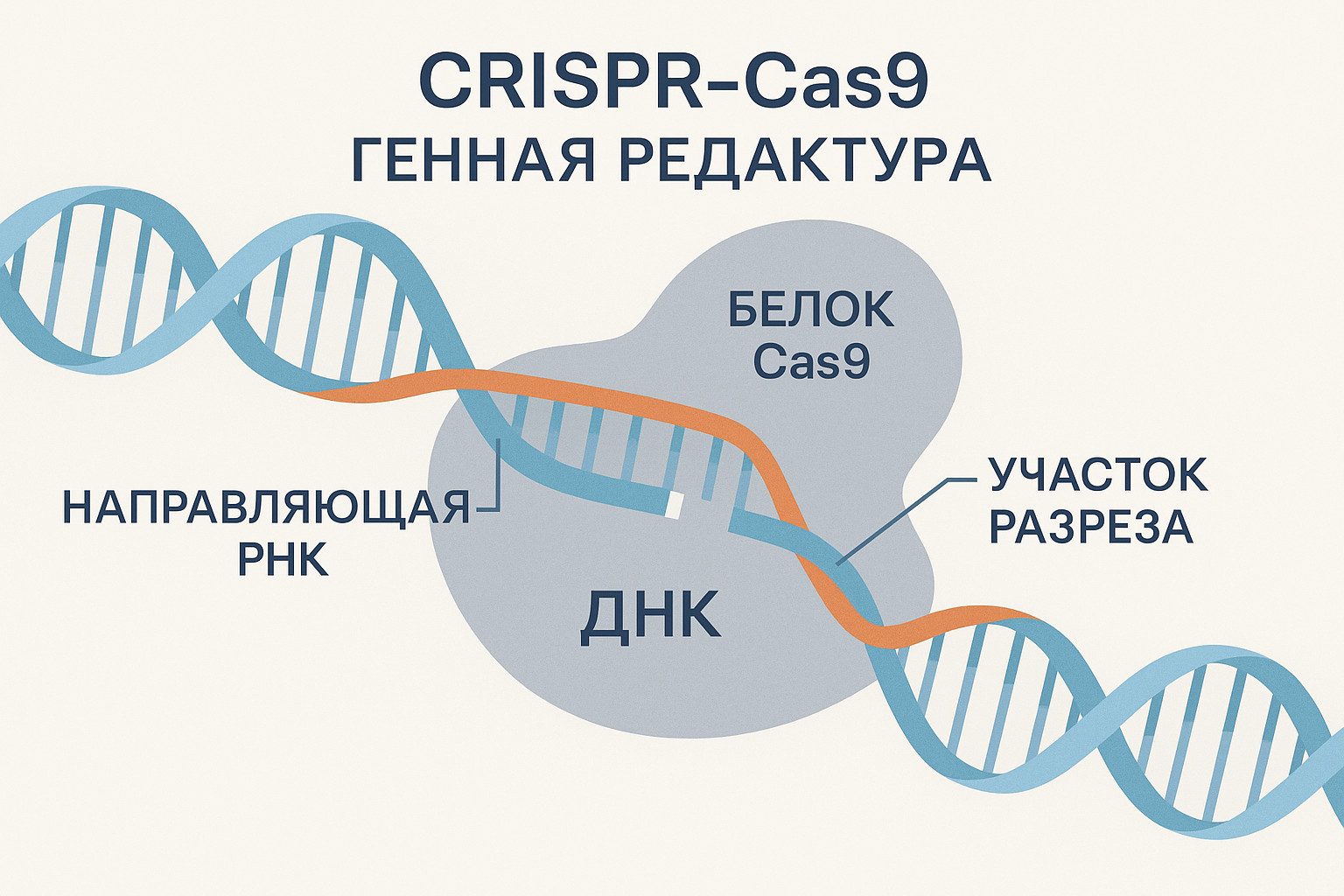
Лекарство из пробирки
Самое очевидное, что принесло CRISPR — возможность точечного вмешательства в ДНК. Если раньше лечение генетических болезней больше напоминало войну с симптомами, то теперь можно бить точно в цель.
Например, наследственные заболевания вроде серповидноклеточной анемии, амилоидоза или бета-талассемии теперь реально лечить не пожизненными курсами лекарств, а раз и навсегда — одной процедурой редактирования генома. Уже в 2023 году в мире зарегистрировали первую официальную CRISPR-терапию для серповидноклеточной анемии. И это не эксперимент — это полноценное лечение, которое получили обычные пациенты.
Работает это так: из организма человека берут стволовые клетки, исправляют в них "битый" ген и возвращают обратно. Исправленные клетки начинают работать правильно, а симптомы болезни постепенно исчезают. В идеале — навсегда.
Но не всё так просто. Редактирование ДНК — процесс тонкий. Ошибка в одну "букву" может запустить совсем не ту цепочку реакций. Поэтому сейчас учёные очень осторожны: перед тем, как отправить клетку обратно в организм, её проверяют на десятки параметров, чтобы избежать возможных мутаций.
Ещё одна горячая область применения CRISPR — онкология. С помощью технологии учёные перепрограммируют иммунные клетки, чтобы те сами находили и уничтожали опухолевые клетки. Такой подход позволяет обходиться без классической химиотерапии, которая "бьёт" по всему организму.
Сегодня подобные терапии проходят клинические испытания на реальных пациентах. И уже есть случаи, когда рак уходит в долгую ремиссию или даже полностью исчезает. Пока что это дорогое удовольствие, доступное немногим, но технологии дешевеют, а значит — через несколько лет подобное лечение может стать стандартом.
Исправить до рождения?
CRISPR открывает перед медициной куда более спорные перспективы. Речь идёт о вмешательстве в эмбрионы — когда болезнь можно предотвратить ещё до рождения ребёнка.
Самый известный случай — история китайского учёного Хэ Цзянькуя, который в 2018 году объявил о рождении первых в мире детей с отредактированным геномом. Учёный пытался защитить их от заражения ВИЧ, исправив ген CCR5. Скандал был оглушительным: мировое сообщество осудило эксперимент, а самого Хэ отправили за решётку.
Почему такая реакция? Потому что редактирование эмбрионов пока слишком рискованно. Ошибки в геноме могут проявиться не сразу, а спустя годы или даже поколения. А ещё — вмешательство в эмбриональные клетки передаётся по наследству, то есть изменения будут вноситься сразу в будущую популяцию людей.
Сейчас в большинстве стран редактирование эмбрионов запрещено или строго ограничено. Но научный прогресс не стоит на месте. Уже разрабатываются проекты, где планируется использовать CRISPR для лечения тяжёлых наследственных заболеваний на стадии эмбриона, если иначе спасти ребёнка невозможно.
И тут перед обществом встаёт масса сложных вопросов. Кто будет решать, какие гены можно исправлять? Где грань между лечением и "улучшением" человека? Как избежать появления общества генетически модифицированных "улучшенных" людей и "обычных" людей? Эти вопросы пока без ответов, но обсуждение идёт уже сейчас.
Лечение без уколов
Ещё одна перспективная сторона CRISPR — создание новых способов доставки терапии.
Учёные работают над методами, которые позволят доставлять CRISPR прямо в организм без тяжёлых процедур. Например:
- Генетические пластыри — наклеил на кожу, и генная терапия началась. Сейчас такие технологии тестируют на животных.
- Ингаляторы — вдыхание аэрозоля, содержащего CRISPR-компоненты, чтобы лечить болезни лёгких, например муковисцидоз.
- Микроиглы — крошечные иглы, незаметные для человека, которые могут впрыскивать CRISPR в клетки.
Ещё более амбициозная задача — использование CRISPR для борьбы с вирусами.
Американские учёные уже работают над препаратами, которые смогут находить и разрушать ДНК вирусов прямо в организме человека. В теории это позволит не просто лечить вирусные инфекции, а полностью уничтожать возбудителей — например, герпес или даже ВИЧ.
Пока такие препараты находятся на стадии испытаний, но уже первые результаты обнадёживают. Если удастся реализовать эти идеи, то в будущем мы сможем забыть о хронических вирусных инфекциях.
CRISPR — это не просто очередная модная технология. Это настоящий прорыв, который меняет сам подход к медицине. Если раньше врачи лечили последствия болезней, то теперь у нас появляется возможность устранять саму причину — на уровне генов.
Конечно, остаются вопросы безопасности. Конечно, не всё так радужно: редактирование ДНК пока очень дорого, технически сложно и сопровождается рисками. Но развитие идёт стремительно.
Через 10–20 лет медицина может выглядеть совершенно иначе: мы будем исправлять дефекты ещё до рождения, лечить рак без химиотерапии, и избавляться от вирусов без тяжёлых препаратов. И, возможно, именно CRISPR станет основой этой новой эры.
Хотя, как обычно бывает с большими открытиями, многое зависит не только от науки, но и от того, как с ними распорядится человечество.